近十年来,平均每隔两三年,中国疫苗领域就会爆发一次影响广泛的事件。这些疫苗安全事件,无论其严重程度还是发生频率,在当今世界,都闻所未闻。7 月 15 日爆出的长春长生疫苗丑闻,更是引起中国最高领导层的关注。
我们不禁要问,这类公共卫生事件,为何唯独在中国屡屡出现,甚至在国家高层的关注之下仍然屡禁不止?
中国疫苗监管法规和标准堪比欧美。然而,这些规章制度有时并未得到疫苗生产企业有效和认真执行;在疫苗监管过程中存在权力寻租现象,一些违法行为甚至受到地方保护主义的庇护;在疫苗销售和采购环节有腐败行为;对疫苗生产商违法违规案件的处罚过轻从而导致违法成本极低以至于劣币驱逐良币。
这些都是中国重塑公众对本土疫苗信心而亟待解决的问题。但是,在这些被热议的问题之外,是否还有其他被忽视的原因?
一则读者来信对比分析了中美在疫苗监管中的一些措施。作者指出:
美国对疫苗偶合事件受害者的依法「无过错」赔偿,对不良反应事件及时、公开的披露,对市场的培育,在一定程度上保障了药企在这一特殊市场中的利益,从而在源头上保证了疫苗质量。
近年来,中国国产疫苗屡曝丑闻,其在安全性方面有诸多不尽人意之处。笔者试图从中国和欧美的对比中发现可能被我们忽略的深层次问题,并提供一些建议以重塑信心。
两个近似
1. 批准上市的机制
中国对疫苗的管理以《药品管理法》为基础,并辅以一系列 CFDA 出台的法规和指南。在生产质量和合规性和新疫苗上市审批方面,中国和美国没有显著差异(图 1)。与欧盟和美国相似,CFDA 也根据批准的疫苗质量标准,汇总编纂了药典,以规定疫苗的质量。
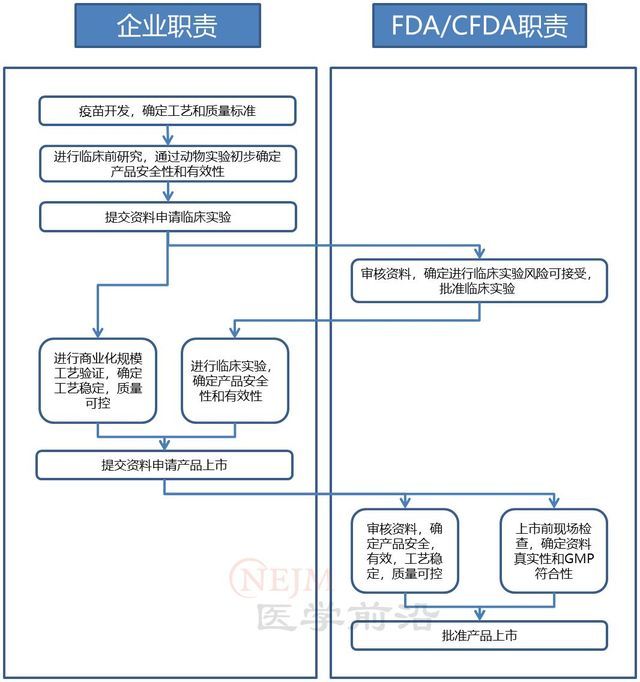
图 中国和美国疫苗上市流程
2. 检测标准
一个鲜为人知的事实是,虽然中国的疫苗产业起步较晚,但药典中规定的很多疫苗标准并不低于欧盟。
笔者对比了两部药典对 8 种重要疫苗的规定,发现中国药典的疫苗检定项目均多于欧盟药典,而且大部分疫苗均有若干个检项标准高于欧盟(表 1)。与欧美国家相同,CFDA 通过派出检查小组前往企业,实施 GMP 检查来确保企业上市后疫苗质量。
2011 年 CFDA 疫苗监管系统通过世界卫生组织的认可,2017 年中国加入人用药品注册技术国际协调会议(ICH),表明中国疫苗监管已与国际接轨。本次长生疫苗事件通过飞行检查发现并公之于众,也从侧面说明了监管系统的有效性。
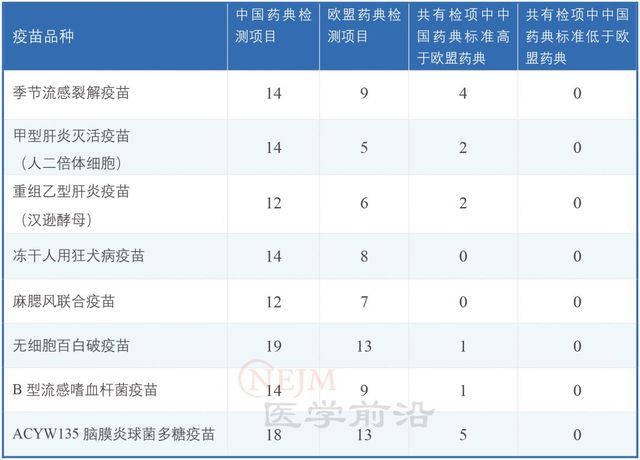
表 中国和欧盟药典检项标准对比
三个差别
1. 疫苗风险管控
由于上文提及的疫苗制品特殊性,美国于 1986 年通过了《国家儿童疫苗伤害法》(NCVIA),对因疫苗接种导致的不良事件受害者给予赔偿,而赔偿金来自美国政府对疫苗的征税。该法案既保障了疫苗接种者的基本权益,又能保证疫苗供应商的积极性。
与美国不同的是,中国疫苗不良反应的具体赔偿没有法律支持,虽在部分国家文件有相关规定,但这些规定又指出补偿办法由省级政府自定,而省级政府又往往未出台具体补偿办法,或虽有补偿,但又存在补偿金额过低,仅有一次性经济补偿等问题,无法切实保障严重不良反应接种者的权益。公众对个别不良反应案例的悲惨境况印象深刻,导致接种疫苗的风险被夸大。
2. 药企利润空间
与任何其他药物一样,研究开发疫苗是一项时间长、投入高、风险高的工作。对比中美疫苗价格(数据来源于 2018 年 7 月 25 日访问的 www.cdc.gov,以及 2017 年中国甘肃省和广西壮族自治区政府招标公示),我们可以发现,在一类疫苗中,中国国产全部 13 种疫苗均价为 13.3 元/支(中位数 7.65;人民币元,下同),而美国全部 20 种疫苗均价为 421 元/支(中位数 375);在二类疫苗中,中国国产全部 22 种疫苗均价为 95 元/支(中位数 74.5),而美国全部 20 种疫苗均价为 608 元/支(中位数 573)。中美疫苗价格差异可达数十倍。
在这样的压力下,中国本土疫苗企业更容易选择造假以降低成本,一旦爆出丑闻,会严重影响公众对本土疫苗的信心和接受程度。当然,低价格绝不是造假的借口,一个有良知的企业应该以质量取胜。
3. 信息发布透明度
疫苗是一项知识密集型产品,其生产、质量控制和效果评价涉及生物技术、分析化学和临床医学等多方面专业领域,公众很难具备以上专业领域知识从而对疫苗的风险和收益自行得出科学合理的判断。
由于疫苗属于处方药,中国禁止以广告或其他方式对公众进行宣传,也在一定程度上加深了厂家和接种者的信息不对等度,容易产生不信任。公众对于未知事物容易产生抵触心理,影响疫苗接受程度。
此外,中国虽有不良反应监测系统,但数据集中在各级疾病控制中心,公众或媒体难于获取,对疫苗的不良反应缺乏全局性的理解和把握,而严重不良反应事件自身容易成为热点,使公众以点代面,产生恐惧心理和对疫苗的抵制。
多管齐下,彻底扭转疫苗公共危机高发的态势
看差别,提建议
从立法层面建立疫苗风险管控制度
目前,中国已有部分疫苗生产厂家针对自己生产的疫苗为接种者免费购买保险,或由部分地区政府购买保险,但这仍只是个案。如果可以吸取美国出台的《国家儿童疫苗伤害法》和国家疫苗伤害赔偿项目,从疫苗价格中征收一部分金额,用于支付疫苗接种者的不良反应,将极大地减少疫苗接种者的后顾之忧,使他们更加乐于接受疫苗。
加大对疫苗产业的投入,保障企业合理的利润空间
中国可参考美国儿童疫苗项目,对贫困家庭的儿童接种二类疫苗提供援助,降低由于经济原因而放弃疫苗接种的情形。此外,适当放开疫苗价格,减轻厂家成本压力,使厂商乐于投入资金研究开发新疫苗,改进工艺,提升现有疫苗质量。
建立疫苗不良反应监控系统,公开透明发布数据
信息不对称容易使公众产生忧虑和不信任。如果政府投入资源,像美国 CDC 一样建立广泛的疫苗不良反应监控系统并对公众开发数据,使接种者可以通过大数据了解疫苗的安全性,破除极个别不良反应事件的影响。
应对公共危机,需要提升社会公共关系的管理能力
我们应该通过高水平的临床研究,研究并解决疫苗的安全性问题。
可以充分发挥各种媒体、科研机构和医师学会等的科普力量,向公众传播疫苗知识,帮助他们从科学的角度理解疫苗的科学原理、质量管理以及安全性和有效性。
制定政策,鼓励医护工作者特别是社区医生接受疫苗相关培训,并与接种者沟通信息,帮助他们分析疫苗的风险和获益,使其认可疫苗是最有效防控特定疾病的手段,从而乐于接种疫苗。
笔者相信,在加强执法和监管力度的基础上,通过以上措施,国产疫苗的质量和安全性可以得到极大地提高,从而保障公众特别是儿童的健康。